测试结果
去屑活性成分
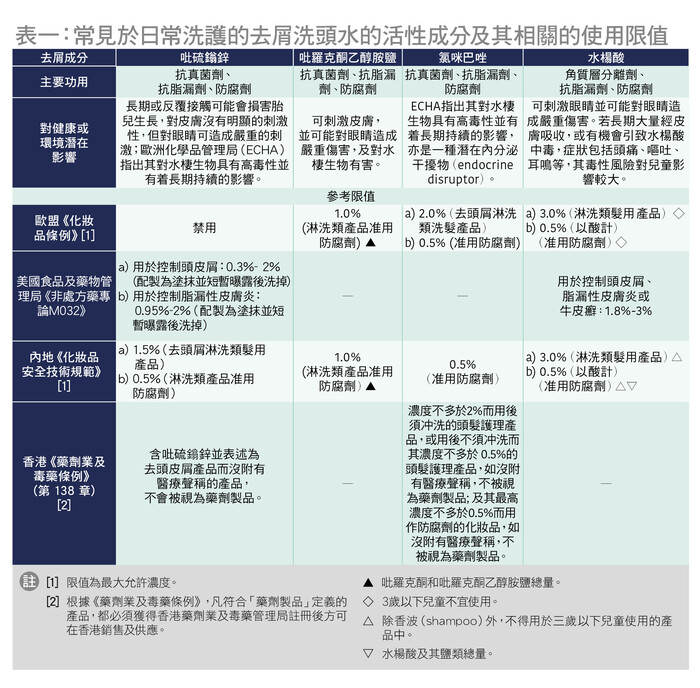
是次测试4种的去屑活性成分,其主要功效和对健康及环境的潜在影响可见表一。不同地区对该等去屑活性成分各有规管,部分地区例如美国或会视相关去屑洗头水产品为非处方药物,规定可用于控制头皮屑的有效成分及其含量。测试结果显示,25款样本中有4款(约1成半)检出吡硫鎓锌,13款(约5成)检出吡罗克酮乙醇胺盐,5款(2成)检出氯咪巴唑,以及10款(4成)检出水杨酸。就是次测试结果而言,可见吡罗克酮乙醇胺盐为较常用于日常洗护的去屑洗头水的活性成分,而使用吡硫鎓锌和氯咪巴唑作为去屑成分的样本则相对少。此外,25款样本中有3款没有检出是次测试的去屑活性成分,包括「KLORANE」(#1)、「MARO」(#11)和「桂圆美」(#15),当中「KLORANE」(#1)和「桂圆美」(#15)声称添加草本或其他成分作为去屑成分。其余22款检出1至3种是次测试的去屑活性成分。
去屑洗头水能否达到理想的去屑功效,取决于多个因素。第一,由于引起头皮屑的原因复杂,要先厘清成因才能对症下药,拣选针对性的去屑成分。第二,去屑活性成分要达到一定有效浓度才能发挥其功效,而去屑洗头水的配方可能同时含有不同的活性成分。第三,产品能否达到一定的去屑功效亦要考虑当中不同成分的加乘效果。第四,是次测试只包括4种较常见的去屑活性成分,未必能涵盖市面上所有相关产品的去屑成分种类。因此是次测试只针对样本中的去屑成分的化学安全性及其含量是否符合相关地区法规的要求为评分准则。
何谓非处方药物?
非处方(over-the-counter,简称OTC)药物,通常用于治疗或纾缓轻微病征,而其副作用也较少。
香港卫生署负责监管所有在香港销售的药物,以确保其安全、成效和素质。非处方药剂制品受《药剂业及毒药条例》(第138章) 规管,「药剂制品」必须获得香港药剂业及毒药管理局注册后方可在香港销售。
在美国,非处方药物受FDA监管,非处方药专论规定了活性成分(active ingredient)、用途或适应症(indications)、剂量(doses)、给药途径(routes of administration)、标签(labelling)和测试(testing)等条件;《非处方药专论M032》(U.S. FDA OTC Monograph M032)规管适合局部使用的非处方头皮屑、脂漏性皮肤炎或牛皮癣药物产品,包括洗头水。如果产品满足该专论的要求,通常被认为是安全有效的。
4款检出欧盟禁用吡硫鎓锌
吡硫鎓锌曾被广泛使用于淋洗类发用产品超过40多年,是常见的抑菌去屑成分,透过抑制引致头皮屑的马拉色菌(Malassezia)的生长以减少头皮屑的产生;同时,它可减慢头皮角质细胞更新,从而抑制头皮屑的增长。然而,吡硫鎓锌对眼睛具有刺激性,ECHA亦将其归类为1B类的CMR物质–致生殖毒性(toxic for reproduction),长期或反复接触可能会损害胎儿生长。2020年欧盟消费者安全科学委员会(简称SCCS)表示,以最大浓度为1%吡硫鎓锌作为淋洗类发用产品的去屑成分基本上是安全的,但该委员会指其用途并非不可替代,因此无法满足CMR物质在化妆品中使用「成分本身无可替代」的豁免条件。因此,其自2022年3月起在欧盟被禁止使用于化妆品中。市场上含吡硫鎓锌的去屑洗头水也因而减少。现时,内地《化妆品安全技术规范》规定去头屑淋洗类发用产品中吡硫鎓锌的最高允许使用浓度为1.5%。此外,吡硫鎓锌是美国食品及药物管理局(FDA)准用的非处方药用成分,其可用于控制头皮屑淋洗类产品的浓度为0.3%至2%,而其可用于控制脂漏性皮肤炎淋洗类产品的浓度为 0.95%至2%。
测试结果显示4款样本,包括「HAIR CORNER」(#21)、「Petal Fresh Pure」(#23)、「CLEAR」(#24)和「Philip B.」(#25)检出吡硫鎓锌,含量由0.19%至0.95%。尽管吡硫鎓锌为欧盟《化妆品条例》的禁用物质,是次样本的检出量仍符合内地《化妆品安全技术规范》的规定。
吡罗克酮乙醇胺盐为最常见去屑活性成分
吡罗克酮乙醇胺盐为新型去屑剂,具有抗真菌和抑制头皮角质细胞增生的作用。因为其毒性较上述的吡硫鎓锌低,所以逐渐取替吡硫鎓锌,成为目前市场上较常用于日常洗护的去屑洗头水的活性成分。根据欧盟和内地规定,吡罗克酮乙醇胺盐为准用防腐剂,于化妆品中的淋洗类产品的最高使用浓度为1.0%。
是次测试,13款样本检出吡罗克酮乙醇胺盐,含量由0.066%至0.86%,全部符合欧盟和内地的规定。
氯咪巴唑浓度符合规定
氯咪巴唑为抗真菌剂,产品可能会同时加入吡硫鎓锌,结合使用以达到额外的抗真菌效果。然而,ECHA于2019年指出氯咪巴唑有可能干扰鱼类的内分泌系统,目前正在评估其内分泌干扰(endocrine disruption)特性。此外,氯咪巴唑对水栖生物毒性极大,并对水的环境有着长期持续的影响。由于氯咪巴唑不易被生物降解,而每日使用含有关成分的洗头水,可能会持续地将含有氯咪巴唑的污水排放到环境中,或会从而污染食物链。根据欧盟和内地规定,氯咪巴唑为准用防腐剂,用于一般化妆品中的最大使用浓度为0.5%;而用于去头屑淋洗类洗发产品,欧盟则规定其使用浓度上限为2.0%。
是次测试结果显示5款样本含氯咪巴唑,检出量由0.048%至0.45%,全部符合欧盟和内地的规定。

「雅浓有机」(#17)标示可控制头皮屑和脂漏性皮肤炎症状。
水杨酸为角质层分离剂
水杨酸可作为角质层分离剂(keratolytic agent),主要可透过去除角质层部分的死皮细胞从而改善头皮屑的症状(如鳞屑和片状皮屑或发炎),而非根治引致头皮屑的相关炎症或疾病。水杨酸是美国FDA准用的非处方药用成分,可用于控制头皮屑、脂漏性皮肤炎和牛皮癣,规定使用的浓度为1.8%至3%。而欧盟和内地规定化妆品中的淋洗类发用产品的水杨酸最高使用浓度为3.0%,此外,水杨酸及其盐类(包括水杨酸钠(sodium salicylate))亦可用作防腐剂,使用浓度上限为0.5%(以酸计),欧盟规定水杨酸不得用于3岁以下儿童使用的产品中,及产品须印有相关警告标示。
是次结果显示,10款样本检出水杨酸,含量由0.087%至1.90%。全部样本的水杨酸含量均符合欧盟和内地的规定。检视产品成分资料,5款样本标示含水杨酸,包括「BIODERMA」(#3)、「巴黎欧莱雅」(#4)、「APIVITA」(#14)、「雅浓有机」(#17)和「KÉRASTASE」(#18),有4款样本标示含水杨酸钠,包括「多芬」(#9)、「THE BODY SHOP」(#16)、「海伦仙度丝」(#20)和「CLEAR」(#24),另「DR ZERO」(#10)未有说明相关成分资料。「雅浓有机」(#17)检出的水杨酸含量为所有样本中最高,含1.90%,达到美国FDA用以控制头皮屑、脂漏性皮肤炎或牛皮癣的非处方药用成分规定的使用浓度范围之内。故此,如于当地售卖,理应会被归类为非处方药物。而其余9款检出的水杨酸含量由0.087%至0.44%,这9款样本同时检出其他抗真菌的去屑成分。
去屑成分有机会刺激皮肤或眼睛
长期或反复接触去屑成分,例如吡罗克酮乙醇胺盐,可能会刺激皮肤,引起泛红和搔痒等过敏反应的症状,而吡硫鎓锌、吡罗克酮乙醇胺盐和水杨酸亦可能刺激眼睛。
研究指出使用含吡硫鎓锌的洗头水可引起接触性皮肤炎,甚或伴有脓疱性牛皮癣(pustular psoriasis)。2010年台湾一项研究指出,1名男性在使用含吡硫鎓锌的洗头水后,头皮、脸部、颈部和手部出现搔痒性皮疹,斑贴测试(patch testing)显示患者对吡硫鎓锌呈阳性反应。另外,2005年韩国一项研究指出,1名患有牛皮癣的患者使用含吡硫鎓锌的洗头水后20天内头皮出现严重的鳞状红斑(erythematous patch),同时双手前臂出现了脓疱性牛皮癣,斑贴测试显示患者对吡硫鎓锌有过敏反应。
使用含吡硫鎓锌、吡罗克酮乙醇胺盐或水杨酸的去头皮屑洗发用品时,消费者应避免洗头水接触到眼睛,以防当中具刺激性的成分损害眼睛。如有洗头水进入眼内,应立即用大量清水冲洗。另外,若使用后出现过敏反应,例如起疹、红斑、肿胀、或发痒等,应立即停用;若症状持续,应谘询医生。消费者亦应细阅产品使用说明,按建议的使用次数和驻留时间使用,以达到最佳效果,并避免洗头水驻留太久而造成刺激反应。因病理性因素而引起头皮屑的患者更应特别小心拣选洗头水及其他个人用品,建议在使用前应先谘询医生意见。
化学安全测试
香料致敏物
香料成分可能源自天然植物萃取物或合成香料,用以掩盖部分原料难闻的气味之余,亦可透过香气提升使用时的感观享受,所以被广泛用于化妆品和护肤品,以吸引消费者购买。然而,研究发现香料成分可能是过敏性接触性皮炎(allergic contact dermatitis)的原因之一。在接触过量香料致敏物质时,身体可能会产生接触性过敏反应,免疫系统会对相关的香料致敏物质产生「记忆反应」。当身体再次接触到该等香料致敏物质时,有机会引起不同的症状,例如过敏性接触性皮炎、红疹等。过敏性接触性皮炎是一种发炎性皮肤病,其特征是皮肤出现红斑(erythema)、肿胀(swelling)和水疱(vesicles)。如继续接触致敏原,可能会发展成慢性疾病,伴随鳞屑、结痂和皮肤出现疼痛的裂痕等症状。
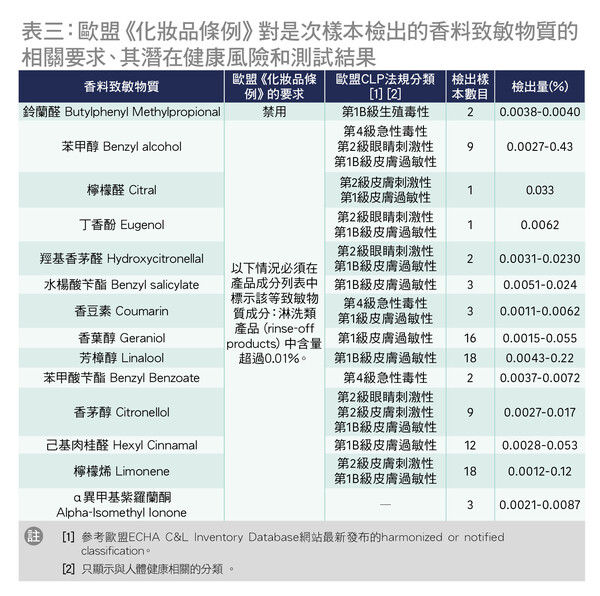
欧盟《化妆品条例》规定了28种常见香料或香料致敏物质(fragrance allergens)的使用要求,当中有4种列为禁用物质,不能添加于化妆品和护肤品之中;而另外24种达特定浓度时,产品供应商便须在标签标示。此规定可让消费者明确知道产品是否添加了相关香料致敏物质,透过避免或限制接触致敏原以达到初级预防(primary prevention);以及避免再次诱发过敏人士产生过敏性接触性皮肤炎来达到二级预防(secondary prevention)。以淋洗类护理用品(rinse-off product)而言(包括去屑洗头水),若该些物质在产品中的浓度超过0.01%,便要标示在成分列表内(详见表三)。
2款样本检出欧盟禁用香料
测试结果显示,25款样本中,只有2款没有检出相关的香料致敏物质,包括「KLORANE」(#1)和「施巴」(#2)。有2款样本检出欧盟禁用的香料铃兰醛(butylphenyl methylpropional,BMHCA,又名Lilial),包括「HAIR CORNER」(#21)和「曼秀雷敦男士」(#22),含量分别为0.0038%和0.0040%。铃兰醛是已知的接触性致敏物质,欧盟同时将其归类为1B类CMR的物质–致生殖毒性,在动物实验结果显示其可影响成年动物的性功能和生育能力。
逾9成样本检出香料致敏物
除了检出欧盟禁用的香料外,23款样本检出1种至7种香料致敏物质,检出量由0.0011%至0.43%。除「BIODERMA」(#3)和「KUNDAL」(#7)检出的香料致敏物质均低于0.01%外,其余21款样本都检出1种至5种含量高于0.01%的香料致敏物质。惟检视样本包装上的成分列表,只有8款有标示该等成分,包括「巴黎欧莱雅」(#4)、「沙宣」(# 5)、「吕」(#12)、「潘婷」(#13)、「APIVITA」(#14)、「THE BODY SHOP」(#16)、「雅浓有机」(#17)和「KÉRASTASE」(#18)。另外,13款没有标示香料致敏物质或只标示部分香料致敏物质,包括「万宁」(#6)、「丽仕」(#8)、「多芬」(#9)、「DR ZERO」(#10)、「MARO」(#11)、「桂圆美」(#15)、「Essential」(#19)、「海伦仙度丝」(#20)、「HAIR CORNER」(#21)、「曼秀雷敦男士」(#22)、「Petal Fresh Pure」(#23)、「CLEAR」(#24)和「Philip B.」(#25),建议厂商改善成分标示,增加产品资迅透明度。
若以检出香料致敏物质的总量计算,检出量由0.0039%至0.4515%,当中总量高于0.1%的9款样本中有5款含苯甲醇(benzyl alcohol)。苯甲醇亦可作为化妆品的防腐剂,欧盟和内地的最大允许使用浓度为1.0%。全部样本所检出的苯甲醇含量都符合相关规定。另外,是次测试发现分别有18款样本检出芳樟醇(linalool)和柠檬烯(limonene),为最常见的香料物质;这两种物质会在接触空气后氧化(oxidation),形成致敏性较高的物质,例如氢过氧化物(hydroperoxides)等,继而出现皮肤过敏的风险。
虽然现时本港法例未有禁用相关香料物质及规定化妆品必须标示详细成分表或列出致敏成分,本会建议有关生产商应留意国际间就香料物质而订定的最新法规和建议,并积极改善产品配方和标签资料,避免使用禁用的化学物质及提供清晰的成分资料,以提示消费者,从而避免可能会出现的致敏风险,并加强对消费者的健康保障。
人造麝香物质
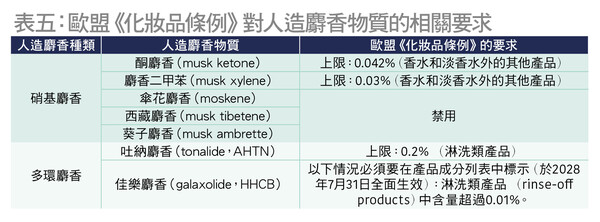
人造麝香模仿天然麝香的气味,常用于个人护理产品作为香料或香料成分。由于这些香料的成分大都是商业机密,因此很少列在标签上。硝基(nitro-musks)及多环麝香(polycyclic musks)类物质难以被降解,可能长时间存在于自然环境中,亦可能积累在动物和人体脂肪中。2007年美国一项研究表示在人类母乳检出这些物质,并指出主要的曝露来源可能是透过皮肤吸收或吸入。韩国、德国和内地等地亦有类似研究在母乳或血液等样本检出这些物质。是次测试了常见于个人护理用品的5种硝基麝香和2种多环麝香,详见表五。
约3成样本检出人造麝香
是次测试发现,全部样本没有检出5种硝基麝香,包括欧盟禁用的伞花、西藏和葵子麝香,以及限用的酮麝香和麝香二甲苯。另外,8款样本检出佳乐麝香,含量由 0.0025%至0.160%,当中6款的检出量超出0.01%,包括「万宁」(#6)、「KUNDAL」(#7)、「潘婷」(#13)、「Essential」(#19)、「海伦仙度丝」(#20)和「HAIR CORNER」(#21)。根据欧盟《化妆品条例》在2023年订下的修定要求,佳乐麝香被列为限用香料致敏物质,如含量超过0.01%须要标示在成分列表内,并将于2028年7月31日全面生效,这6款样本检出的佳乐麝香理论上已达到欧盟须作相关标示的含量。惟检视各产品标签,均未有标示相关资料,现阶段虽为相关修定的过渡期,本会仍鼓励厂商不时留意国际间就香料物质而订定的最新法规和建议作出改善。另外,「潘婷」(#13)同时检出吐纳麝香,含量为0.016%,符合欧盟淋洗类护理用品订定的上限(0.2%)。
佳乐麝香为潜在内分泌干扰物,另外,佳乐麝香和吐纳麝香对水栖生物毒性极大,并对环境有着长期持续的影响。这类物质在各种消费品中广泛大量使用,会积累在海洋生态和自然环境中,最终可能会污染食物链。因此,虽然香港未有相关法例,本会仍建议厂商检示产品配方,改用其他对环境影响较低的香料成分。
约1成半样本检出二恶烷
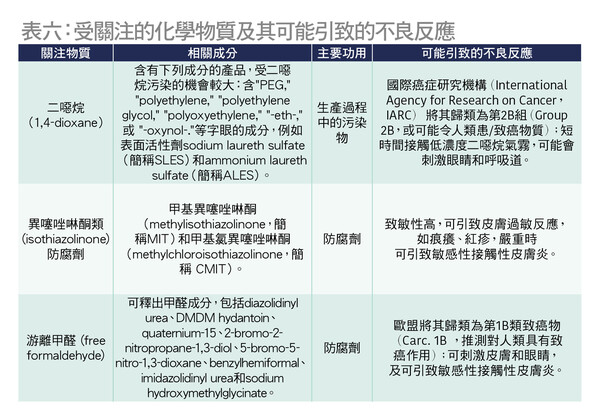
二恶烷(1,4-dioxane)是一种潜在的致癌物,美国卫生与公众服务部(U.S. HHS)在2012年发表的一份报告指出,短时间接触低浓度二恶烷气雾可能会刺激眼睛和呼吸道。根据欧盟《化妆品条例》和内地《化妆品安全技术规范》2015年版的要求,二恶烷不可用于化妆品中。如属非刻意添加而技术上无法避免,化妆品中含有微量二恶烷是允许的,内地要求限值为30ppm; 欧盟SCCS在2015年12月的报告提出,化妆品成品中二恶烷的含量低至10ppm或以下属于安全水平。
本会于2017年进行的洗头水测试,发现有逾6成样本检出二恶烷,而当中1成的二恶烷含量高于欧盟SCCS的建议水平。是次测试的25款样本中,有5款(2成)样本检出二恶烷,包括「吕」(#12)、「APIVITA」(#14)、「桂圆美」(#15)、「THE BODY SHOP」(#16)和「曼秀雷敦男士」(#22),检出量由1.2至2.0ppm,全部符合欧盟SCCS的建议水平和内地的要求限值,可见近年生产商致力于改善其生产过程并监控品质以进一步降低产品的二恶烷含量。纵使是次检出的二恶烷含量对消费者的日常使用不会构成安全威胁,本会仍鼓励相关生产商继续改善其产品的生产流程及原材料,以达致不含二恶烷的水准。
1款样本检出可致敏防腐剂 CMIT
「甲 基 异 噻 唑啉酮」(methyl-isothiazolinone,M I T)和「甲 基 氯 异 噻 唑 啉 酮」(methylchloroisothiazolinone,CMIT)等防腐剂可能令人过敏。根据欧盟《化妆品条例》规定,MIT只可用于淋洗类产品,而其含量不能超过0.0015%。CMIT/MIT混合物的浓度上限同为0.0015%(混合比例以3比1计)。如产品配方已使用CMIT/MIT混合物,则不可额外添加MIT作为防腐剂。本会于2017年进行的洗头水测试,发现有2成样本检出MIT及/或CMIT(总量由0.00054%至0.00994%)。是次测试样本中,只有「桂圆美」(#15)检出CMIT,检出量为0.00092%,样本并没有检出MIT,故此,检出的CMIT/MIT混合物总量符合欧盟的上限规定。本会检视其标签资料,发现样本只以中文标示部分成分资料,没有标示添加CMIT。另外有3款样本,包括「沙宣」(#5)、「潘婷」(#13)和「Philip B.」(#25)则标示有添加CMIT及MIT,惟测试并没有检出CMIT及MIT,相信是因为其含量低于检测限值所致。是次结果显示近年生产商已改善配方,或以其他较低致敏性的防腐剂代替CMIT/MIT。
全部样本没有检出游离甲醛
以往甲醛(formaldehyde)在化妆品中可用作防腐剂,但近年已被欧盟和内地列为禁用物质。此外,一些防腐剂属于甲醛释放剂(formaldehyde releaser),欧盟在2022年7月30日规定如化妆品含有特定可释出甲醛成分而甲醛浓度超过0.001%,其包装必须印有警告语标示产品「释出甲醛」。是次测试结果显示,全部样本都没有检出游离甲醛,情况令人满意。
标签资料
成分列表
检视样本的标签资料,发现4款样本没有在标签上以中文或英文列出成分资料,只说明去屑活性成分,包括「DR ZERO」(#10)、「MARO」(#11)、「Essential」(#19)和「曼秀雷敦男士」(#22);以及1款样本「桂圆美」(#15)只标示部分成分资料。
在去屑活性成分资料方面,所有检出去屑成分的产品均有说明相关资料供消费者参考,情况理想。
至于香料致敏物质方面,只有约4成样本完整标示相关成分。由于患有头皮屑问题人士的头皮或已出现过敏情况,所以建议厂商积极完善产品的标签资料,增加其资讯透明度,让消费者能知所选择。
使用期限
6款样本只标示有效期限;另有13款同时标示有效期限和保质期/开封后使用期,标示方法较详尽;只有1款(「万宁」(#6))产品同时标示生产日期、有效期限和开封后使用期,资料最全面,让消费者按需要可以选购较近期制造的产品,在限期前使用,并在开封后使用期内尽快用完。
安全提示
按欧盟规定,含水杨酸的产品需于标签上印有「三岁以下儿童勿用」的警告标示。10款检出水杨酸的样本中,4款的成分列表标示含水杨酸钠,另有5款标示含水杨酸,当中只有「巴黎欧莱雅」(#4)有作出相关警告标示;「BIODERMA」(#3)则提示「产品仅供成人使用」;而其余4款样本,包括「DR ZERO」(#10)、「APIVITA」(#14)、「雅浓有机」(#17)和「KÉRASTASE」(#18)等均没有任何相关警告标示,建议厂商积极完善产品的安全提示。